ঈথার
ইংরেজি Ether।
ঊনবিংশ শতাব্দীর জ্যোতিষী ও পদার্থবিদগণ কল্পনা করতেন যে- ঈথার নামক একটি ভরহীন ও
আদর্শ স্থিতিস্থাপক বস্তু সমগ্র বিশ্ব ব্রহ্মাণ্ড জুড়ে অবস্থান করছে। এই ধারণা
দীর্ঘকাল ধরে প্রচলিত ছিল। কিন্তু ঈথারীয় মতবাদে সকল সমস্যার সমাধান না থাকায়- একটি
বড় ধরণের গালমালের সৃষ্টি হয়েছিল। ১৯০৫ খ্রিষ্টাব্দে আইনস্টাইন তাঁর দুটি স্বীকার্য
প্রকাশ করেন। এর দ্বারা একই সাথে ঈথারের ধারণা বাতিল হয়ে যায় এবং আপেক্ষিক তত্ত্ব
প্রতিষ্ঠা পায়।
রসায়নবিদ্যায় ঈথার একপ্রকার যৌগশ্রেণিকে বুঝায়। একটি দ্বিযোজী অক্সিজেন পরমাণুর
সাথে দুটি এ্যালকাইলমূলক যুক্ত হয়ে যে সকল জৈব যৌগ উৎপন্ন করে, সে সকল যৌগসমূহকে
শ্রেণিগত ভাবে ঈথার বলে। দুই অণু এ্যালকোহল মিলিত হলে এবং ওই মিলিত যৌগ থেকে এক
অণু পানি নিরুদিত হলে– একটি ঈথার উৎপন্ন হয়। এই কারণে
অনেকে ঈথারকে ডাই-এ্যালকাইল অক্সাইড হিসাবে চিহ্নিত করে। এর সাধারণ সংকেত-
R-O-R।
এর কার্যকরী মূলক হলো –O–।
ঈথারকে প্রাথমিকভাবে দুই ভাগে ভাগ করা হয়। এই ভাগ দুটি হলো–
- এ্যালিফেটিক ঈথার : বেনজিন-এর
সাথে সম্পর্ক নেই এমন ঈথার। এই জাতীয় ঈথার গঠনানুসারে দুই রকম হতে পারে। এই রকম
দুটি হলো– মুক্ত শিকল ঈথার ও চাক্রিক ঈথার।
-
মুক্ত শিকল ঈথার: এই জাতীয় ঈথারের পরমাণুগুলো শিকলের মতো বিন্যস্ত থাকে।
এর গাঠনিক প্রকৃতি অনুসারে দুটি ভাগে ভাগ করা হয়। এই ভাগ দুটি হলো–
১. সরল ঈথার : যে সকল
ঈথারের অণুতে একই জাতীয় দুটি এ্যালকাইল মূলক থাকে, সে সকল ঈথারকে সরল ঈথার
বলে। সরল ঈথারের সাধারণ সংকেত-
R-O-R।
২. মিশ্র ঈথার : যে সকল ঈথারের অণুতে দুটি ভিন্ন জাতীয় এ্যালকাইল
মূলক থাকে, সে সকল ঈথারকে সরল ঈথার বলে। মিশ্র ঈথারের সাধারণ সংকেত
R-O-R´।
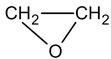
- চাক্রিক ঈথার: এই জাতীয় ঈথারের কাঠামো বলয়াকার। যেমন–
ইথিলিন
অক্সাইড।
- এ্যারোমেটিক ঈথার : এই ঈথারে –O–
যৌগমূলকের প্রান্তে থাকে
এ্যারোমেটিক উপাদান , অন্য প্রান্তে থাকে এ্যালোফেটিক বা এ্যারোমেটিক উপাদান।
এই কারণে গাঠনিক সংকেত উল্লেখ করা হয়
AR-O-R
বা AR-O-AR।
গঠনের বিচারে একে দুটি ভাগে ভাগ করা হয়। এই ভাগ দুটি হলো–
১. সরল ঈথার : যে সকল
ঈথারের –O–
যৌগমূলকের উভয় প্রান্তে থাকে এ্যারোমেটিক উপাদান । এর গাঠনিক সংকেত
AR-O-AR।
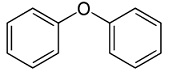
যেমন– ডাই-ফিনাইল ঈথার
২. মিশ্র ঈথার : যে সকল ঈথারের –O–
যৌগমূলকের একপ্রান্তে থাকে এ্যারোমেটিক উপাদান এবং অপর প্রান্তে থাকে
এ্যালোফেটিক। এর সংকেত
AR-O-R।
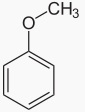
যেমন– মিথাইল-ফিনাইল ঈথার
ঈথারের নামকরণের ক্ষেত্রে দুটি পদ্ধতি
অনুসরণ করা হয়। যথা–
| |
ক. সাধারণ পদ্ধতি : সরল
ঈথারের ক্ষেত্রে সর্বাগ্রে 'ডাই' শব্দটি বসে। যেমন : ডাই মিথাইল ঈথার।
কিন্তু মিশ্র ঈথারের ক্ষেত্রে এ্যালকাইল মূলকের নামের আদি অক্ষর ইংরেজি
বর্ণমালার ক্রমানুসারে লিখে শেষে ঈথার শব্দটি যোগ করা হয়। যেমন: ইথাইল
মিথাইল ঈথার, মিথাইল প্রাপাইল ঈথার ইত্যাদি। |
| |
|
| |
খ. জেনেভা পদ্ধতি : এই
পদ্ধতিতে ঈথারকে এ্যালকেন-এর এ্যাল্কোক্সি উদ্ভূতক রূপে গণ্য করা হয়। দুটি
এ্যালকাইল মূলকের মধ্যে ক্ষুদ্রতর এ্যালকাইল মূলকটি ও অক্সিজেন পরমাণু সহ
সৃষ্ট এ্যালকোক্সি মূলক দ্বারা প্রতিস্থাপিত বৃহত্তর এ্যালকাইল মূলকের
এ্যালকেন' রূপে যৌগটির নামকরণ করা হয়। যেমন– সাধারণ নামের ডাই-মিথাইল ঈথার
জেনেভা পদ্ধতিতে হয়− মিথোক্সি মিথেন। মিথাইল প্রাপাইল ঈথার হবে মিথোক্সি
প্রাপেন। |


